가톨릭대 깅한창 교수 연구팀, 세포·동물 실험서 확인
디셀레나이드가 암세포 만나면 분해되는 원리 이용
항암제 약물 작용 도와 항암시너지 2배 효과 얻어
한국연구재단은 가톨릭대학교 약학대학 강한창 교수 연구팀이 디셀레나이드 기반 약물전달체가 항암제의 작용을 도울 수 있음을 확인했다고 16일 밝혔다.
디셀레나이드(diselenice)는 셀레늄 두 분자가 화학결합한 화합물로 산화 및 환원 조건 하에서 생분해되는 특성이 있다.
자극 감응성 약물전달체는 특정조건에서 스스로 반응해 안에 담겨진 약물을 방출한다. 온도, 산성도, 화학물질, 효소 등 세포의 다양한 물리화학적 자극이나 효소활동 등에 반응, 분해되거나 또는 크기가 변하는 원리다.
디셀레나이드 결합이 포함된 화합물 역시 세포 내 화학물질이자 항산화물질인 '글루타치온'과 활성산소 모두에 의해 분해될 수 있어 자극감응성 약물전달체의 좋은 구성성분이 될 수 있다.
세포 내 활성산소와 글루타치온이 공존하는 만큼 이 둘을 모두 고려한 약물전달체 연구가 필요했다.
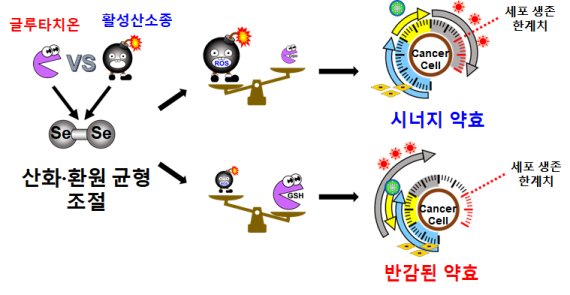
연구진은 활성산소보다 글루타치온이 디셀레나이드를 더 잘 분해하는 것을 알아냈다. 또한 글루타치온이 활성산소보다 더 빠르게 소비되면서 산화스트레스가 가속화되는 것도 알아냈다.
특히 암세포는 활성산소의 산화능과 글루타치온의 항산화능이 모두 정상세포에 비해 상대적으로 높다. 때문에 글루타치온에 의한 디셀레나이드 분해가 정상세포에 비해 더 빠르게 일어나면서 항산화능이 급격히 감소, 산화스트레스로 인해 암세포만 선택적으로 죽게 되는 원리를 알아냈다.
나아가 대장암 생쥐모델을 통해서도 이를 확인했다. 고용량(5㎎/㎏ 2회 주사)의 독소루비신 만을 투여했을 때 보다 저용량의 독소루비신(10분의 1 농도)을 디셀레나이드 약물 전달체에 담아 투여한 경우 종양크기의 감소가 1.9배 더 높게 나타났다.
연구진은 암 뿐 아니라 다른 질병 내의 산화능과 항산화능을 조절해 시너지 약효를 기대, 디셀레나이드 약물전달체의 병용과 관련한 후속연구를 지속할 계획이다.
이번 연구의 성과는 소재 분야 국제학술지 '어드밴스드 펑셔널 머티리얼즈'에 9일 게재됐다.
monarch@fnnews.com 김만기 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지

