관련종목▶
최근 유럽 EMA 허가 획득해 상반기 중 출시 예정
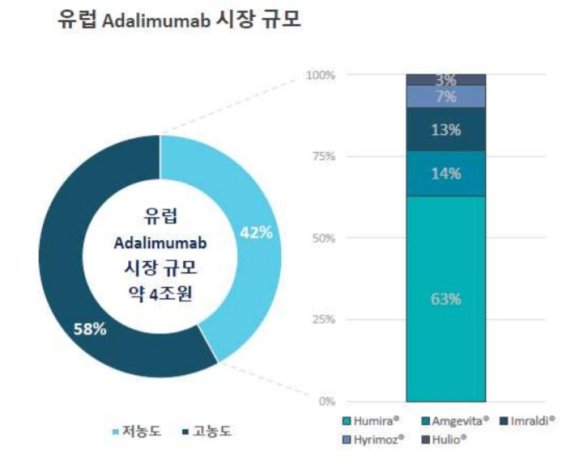
[파이낸셜뉴스] 셀트리온이 세계 최초 고농도 제형의 휴미라 바이오시밀러를 올 상반기 유럽 시장에 선보인다. 셀트리온은 고농도 제형, 가격 경쟁력 등을 바탕으로 퍼스트무버로써 약 4조원 규모의 유럽 시장을 공략한다는 방침이다.
15일 업계에 따르면 셀트리온은 지난 11일(현지시간 기준) 유럽연합 집행위원회로부터 자가면역질환 치료제 휴미라(성분명 아달리무맙)의 바이오시밀러 'CT-P17'에 대해 판매 허가를 받았다. CT-P17은 '유플라이마(YUFLYMA)'라는 브랜드명으로 글로벌 시장에 선보이게 된다.
유플라이마는 셀트리온이 2013년 램시마(류마티스 관절염) 이후 5번째 유럽에 선보이는 바이오시밀러다. 셀트리온은 램시마에 이어 △허주마(2018년 2월) △트룩시마(2017년 2월) △램시마SC(2019년 11월) 등을 유럽에 출시한 바 있다.
셀트리온은 지난해 12월 유럽의약품청(EMA) 산하 약물사용자문위원회(CHMP)로부터 판매 승인 권고 의견을 받은 지 약 2개월 만에 류마티스 관절염(RA), 염증성 장질환(IBD), 건선(PS) 등 휴미라가 보유한 모든 적응증에 대해 판매 허가를 받았다.
유플라이마는 아달리무맙 성분 바이오시밀러로는 세계 최초로 시장에 선보이는 고농도 제형이다. 기존 휴미라 바이오시밀러 제품들이 올드 타입(Old Type)인 저농도로 개발된 데 반해 유플라이마는 뉴 타입(New Type)인 고농도 제형으로, 약물 투여량을 절반으로 줄이고 통증을 유발할 수 있는 시트르산염(Citrate, 구연산염)을 제거해 차별화된 상품성과 높은 시장성을 동시에 확보했다.
유플라이마의 오리지널 의약품인 휴미라는 미국 바이오기업 애브비가 개발한 자가면역질환 치료제로, 지난해 글로벌 매출 약 22조원을 기록하며 글로벌 매출 1위를 차지한 블록버스터 의약품이다. 지난 2015년 애브비가 휴미라 고농도 제형의 유럽 허가를 획득한 이후 현재 유럽에서 판매되고 있는 휴미라의 90% 이상은 고농도 제형인 것으로 집계되고 있다.
유플라이마는 글로벌 마케팅 및 유통을 담당하고 있는 셀트리온헬스케어를 통해 유럽 내 국가별 약가 등재 등의 과정을 최대한 빨리 진행해 시장에 조기 진입한다는 계획이다. 특히, 뉴 타입 휴미라 바이오시밀러는 유럽에서 최초로 선보이기 때문에 셀트리온헬스케어는 '퍼스트무버' 이점을 적극 활용해 경쟁제품 출시 전 시장 점유율을 극대화한다는 계획이다.
셀트리온은 앞으로 램시마(IV, SC) 제품군과 함께 선보일 유플라이마의 탁월한 시장성을 바탕으로 글로벌 자가면역질환 치료제 시장에서 탄탄한 제품 포트폴리오를 구축하게 됐다.
셀트리온 관계자는 "셀트리온은 보다 시장성이 높은 고농도 타입으로 개발에 집중했고 이번 EC 승인으로 유플라이마의 차별화된 경쟁력을 인정받아 유럽에서 세계 최초로 뉴타입 휴미라 바이오시밀러를 선보일 수 있게 됐다"며 "그 동안 뉴타입 휴미라 바이오시밀러를 기다려온 유럽 의료진과 환자들에게 빠른 시일 내에 공급해 고품질 바이오의약품의 혜택을 합리적으로 제공할 계획이다"고 말했다.
hsk@fnnews.com 홍석근 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지

