관련종목▶
1상 통해 안전성과 내약성, 유효성 확인할 예정
[파이낸셜뉴스] 지놈앤컴퍼니는 식품의약품안전처에 신규타깃 항암제 ‘GENA-104’의 국내 임상 1상 시험계획(IND)을 제출했다고 29일 밝혔다.
최대 80명의 고형암 환자를 대상으로 임상을 진행하며, 임상 진행기관은 서울대학교병원을 포함해 두 곳으로 예정됐다.
이번 임상1상은 용량 증량 코호트를 통해 1차 목표인 안전성과 내약성을 입증하고, 유효성에 따라 보충 코호트를 통해 2차 목표인 유효성을 확인할 예정이다.
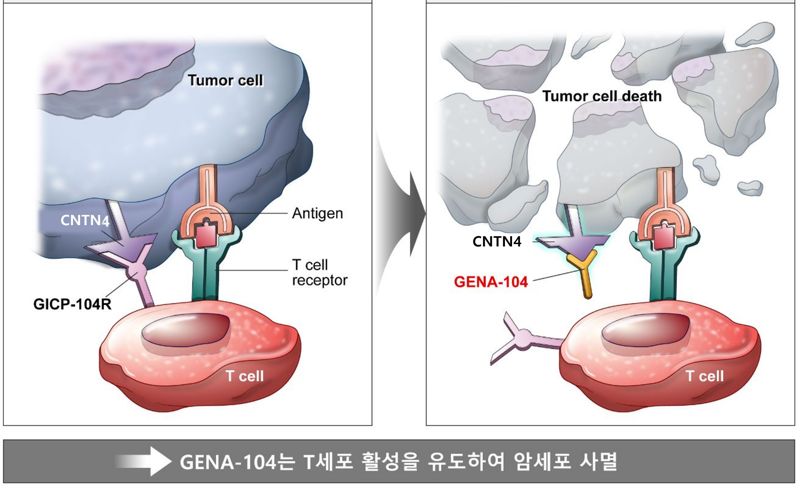
‘GENA-104’는 지놈앤컴퍼니가 자체 플랫폼 GENOCLETM을 통해 세계 최초로 발굴한 CNTN4 단백질을 타깃으로 하는 면역관문억제제다. ‘GENA-104’는 암세포에서 발현되는 단백질 CNTN4가 T세포 활성을 억제하는 것을 차단한다.
지놈앤컴퍼니는 전임상을 통해 CNTN4가 다양한 종류의 암조직에서 과발현 되는 것을 확인했다. CNTN4 발현이 높은 사람들은 PD-L1 발현이 상대적으로 감소한 경향을 보였다.
기존의 승인 받은 PD-(L)1계열 면역항암제는 치료 반응환자가 10~20%로 제한적이기 때문에 이를 충족하기 위한 새로운 항암제에 대한 수요가 절실한 상황이다.
이에 지놈앤컴퍼니는 PD-L1이 발현하는 환자수 대비 CNTN4가 발현하는 환자수가 절대적으로 많고, CNTN4가 과발현하는 경우 PD-L1이 발현하지 않는 배타적 발현 양상을 확인했다. 또 기존 면역항암제에 불응하는 환자에게 새로운 대안 치료제로서의 가능성을 확인했다.
이 전임상 결과는 지난 2021년부터 2023년까지 3년 연속 미국암연구학회(AACR)에서 발표했으며 지난해 국가신약개발사업 과제로도 선정된 바 있다.
배지수 지놈앤컴퍼니 대표는 “’GENA-104’ 전임상을 통해 기존 면역항암제의 비반응군 환자들을 치료할 수 있는 신규타깃 면역항암제로서의 가능성을 확인했다”며 “’GENA-104’가 새로운 면역항암제 시장을 열 것으로 기대되며, 임상 1상에서 경쟁력 있는 결과를 보여줄 수 있도록 연구 개발에 총력을 기울이겠다”고 전했다.
vrdw88@fnnews.com 강중모 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지

