관련종목▶
[파이낸셜뉴스] 엔케이맥스가 내달 개최되는 미국임상종양학회(ASCO)에 제출된 포스터 총 2건을 30일 공개했다.
해당 포스터는 엔케이맥스의 자회사 엔케이젠바이오텍이 진행중인 불응성 고형암(육종암) 임상 1상으로 슈퍼NK(SNK01) 단독투여군, 슈퍼NK+바벤시오(성분명: 아벨루맙) 병용투여군에 임상에 대한 내용이다.
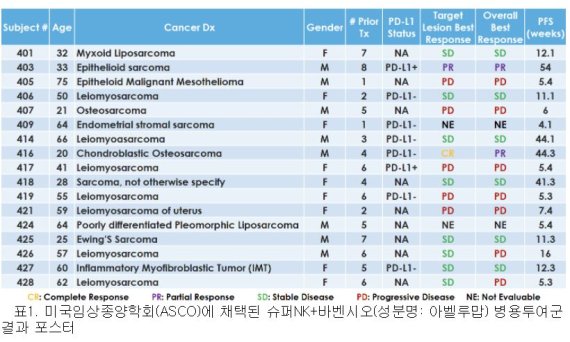
슈퍼NK 단독투여군은 미국에서 진행중인 육종암 임상 코호트1~3 임상 결과다. 기존치료제가 듣지 않는 환자 9명 중 6명이 암덩어리가 더이상 커지지 않는 안전병변(SD: stable disease)로 확인돼 질병통제율(DCR: Disease Control rate) 66.7%을 기록했다. 포스터에 따르면 기존치료제를 최대 9차례 치료를 진행하였으나 전혀 반응을 보이지 않은 환자들에서 NK세포 단독투여만으로 암의 진행이 멈추는 효과를 보여, 안전성 및 유효성을 확보했다는 평가이다. 슈퍼NK와 바벤시오 병용투여군 포스터에는 코호트4에 속하는 총 17명의 육종암 환자에 대한 중간 결과가 공개됐다. 다만 2명에 대한 데이터는 아직 도출해 내지 못해 이번 포스터에는 추가되지 못했으나 최종결과에서 발표 될 예정이다.
이번 포스터에서 병용투여 결과 표적병변에서 완전관해(CR: complete response) 1명, 종양이 30%이상 줄어든 부분관해(PR: partial response)환자가 1명, 종양이 더 이상 자라지 않는 SD(SD: stable disease)환자가 8명 관찰됐다. CR이 확인된 환자의 경우 비표적병변(Non Target Lesion)에 종양이 남아있어 미국 식품의약국(FDA)의 기준에 따라 PR로 초록에 표시됐다. 이 환자는 폐 등 온몸에 암이 퍼져 있는 상태로 임상 환자에 등록돼 슈퍼NK와 바벤시오를 병용투여한 결과 지난해 8월 온 몸의 암이 사라진 CR이 나타났다. 이후 환자를 계속 관찰하던 중 폐에서 소량의 암세포가 관찰되어 이번 학회 초록에는 PR로 제출했다는 것이 회사측의 설명이다. 아울러 해당 환자의 표적병변인 육종에서는 CR상태가 유지된 것으로 확인됐다.
엔케이맥스 관계자는 “CR 확인 환자의 비표적병변(Non Target Lesion)인 폐에서 소량의 종양이 일부 발현됐지만 표적병변인 육종에서는 CR상태가 유지됐다”며 "육종암은 전이될 확률이 매우 높은 악성 종양으로 면억관문억제제를 포함한 기존 치료제가 듣지 않는 말기 육종암 환자에게서 종양 진행이 멈춘 것만으로도 놀라운 결과인데 해당 임상에서는 표적병변 CR상태가 유지되고 있다”라고 말했다. 그는 이어 “이는 슈퍼NK가 새로운 치료법이 될 수 있는 가능성을 입증한 결과"며 "아직 임상이 종료되지 않았기 때문에 금번 중간결과 보다 최종데이터가 더 기대된다"고 강조했다.
kakim@fnnews.com 김경아 기자
※ 저작권자 ⓒ 파이낸셜뉴스, 무단전재-재배포 금지

